Síndrome del dedo azul secundario a ateroembolia por colesterol: reporte de un caso y revisión de la literatura
DOI:
https://doi.org/10.17533/udea.iatreia.v29n2a12Palabras clave:
ateroembolia, embolia por colesterol, síndrome del dedo azulResumen
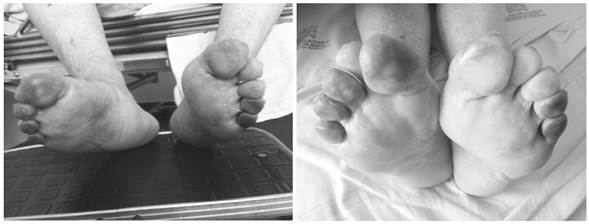
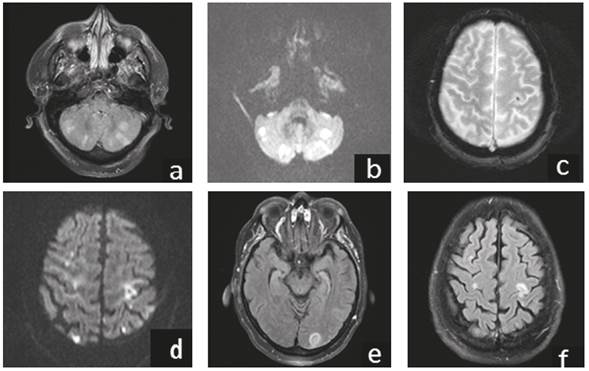
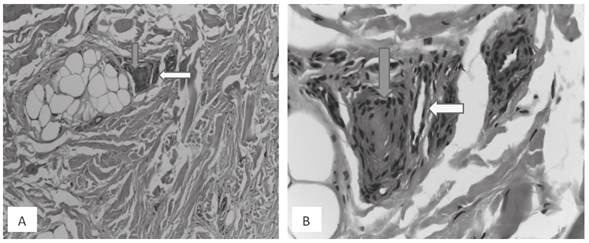
Se describe el caso de una mujer de 68 años, con muy alto riesgo cardiovascular, quien consultó por cianosis en los dedos de los pies, asociada a síntomas neurológicos focales transitorios de 5 días de evolución. Se hospitalizó con la impresión diagnóstica de síndrome del dedo azul e isquemia crítica arterial de miembros inferiores de posible origen embólico. Luego de un procedimiento endovascular, presentó deterioro neurológico súbito y se documentaron múltiples infartos cerebrales y falla renal aguda. En la biopsia de los dedos afectados se observaron cristales de colesterol en el interior de los vasos sanguíneos. Con base en el caso se presenta una corta revisión del síndrome del dedo azul y su principal causa: la ateroembolia.
Descargas
Citas
(1.) Hirschmann JV, Raugi GJ. Blue (or purple) toe syndrome. J Am Acad Dermatol. 2009 Jan;60(1):1-20; quiz 21-2. DOI 10.1016/j.jaad.2008.09.038.
(2.) Saric M, Kronzon I. Cholesterol embolization syndrome. Curr Opin Cardiol. 2011 Nov;26(6):472-9. DOI 10.1097/HCO.0b013e32834b7fdd.
(3.) Tunick PA, Kronzon I. Atheromas of the thoracic aorta: clinical and therapeutic update. J Am Coll Cardiol. 2000 Mar;35(3):545-54.
(4.) Brown PJ, Zirwas MJ, English JC 3rd. The purple digit: an algorithmic approach to diagnosis. Am J Clin Dermatol. 2010;11(2):103-16. DOI 10.2165/11530180-000000000-00000.
(5.) Fukumoto Y, Tsutsui H, Tsuchihashi M, Masumoto A, Takeshita A; Cholesterol Embolism Study(CHEST) Investigators. The incidence and risk factors of cholesterol embolization syndrome, a complication of cardiac catheterization: a prospective study. J Am Coll Cardiol. 2003 Jul;42(2):211-6.
(6.) Harloff A, Simon J, Brendecke S, Assefa D, Helbing T, Frydrychowicz A, et al. Complex plaques in the proximal descending aorta: an underestimated embolic source of stroke. Stroke. 2010 Jun;41(6):1145-50. DOI 10.1161/STROKEAHA.109.577775.
(7.) Heinzlef O, Cohen A, Amarenco P. [Atherosclerotic aortic plaques and risk of embolic stroke]. Rev Neurol (Paris). 2001 Jul;157(6-7):619-31. French.
(8.) Fukumoto Y, Tsutsui H, Tsuchihashi M, Masumoto A, Takeshita A; Cholesterol Embolism Study(CHEST) Investigators. The incidence and risk factors of cholesterol embolization syndrome, a complication of cardiac catheterization: a prospective study. J Am Coll Cardiol. 2003 Jul;42(2):211-6.
(9.) Blackshear JL, Zabalgoitia M, Pennock G, Fenster P, Strauss R, Halperin J, et al. Warfarin safety and efficacy in patients with thoracic aortic plaque and atrial fibrillation. SPAF TEE Investigators. Stroke Prevention and Atrial Fibrillation. Transesophageal echocardiography. Am J Cardiol. 1999 Feb;83(3):453-5, A9.
(10.) Bruns FJ, Segel DP, Adler S. Control of cholesterol embolization by discontinuation of anticoagulant therapy. Am J Med Sci. 1978 Jan-Feb;275(1):105-8.
(11.) Kronzon I, Saric M. Cholesterol embolization syndrome. Circulation. 2010 Aug;122(6):631-41. DOI 10.1161/CIRCULATIONAHA.109.886465.
(12.) Haas M, Spargo BH, Wit EJ, Meehan SM. Etiologies and outcome of acute renal insufficiency in older adults: a renal biopsy study of 259 cases. Am J Kidney Dis. 2000 Mar;35(3):433-47.
(13.) Paraskevas KI, Koutsias S, Mikhailidis DP, Giannoukas AD. Cholesterol crystal embolization: a possible complication of peripheral endovascular interventions. J Endovasc Ther. 2008 Oct;15(5):614-25. DOI 10.1583/08-2395.1.
Publicado
Cómo citar
Número
Sección
Licencia
Derechos de autor 2016 Iatreia

Esta obra está bajo una licencia internacional Creative Commons Atribución-CompartirIgual 4.0.
Los artículos publicados en la revista están disponibles para ser utilizados bajo la licencia Creative Commons, específicamente son de Reconocimiento-NoComercial-CompartirIgual 4.0 Internacional.
Los trabajos enviados deben ser inéditos y suministrados exclusivamente a la Revista; se exige al autor que envía sus contribuciones presentar los formatos: presentación de artículo y responsabilidad de autoría completamente diligenciados.