Epidemiología de Salmonella spp., Listeria monocytogenes y Campylobacter spp., en la cadena productiva avícola
DOI:
https://doi.org/10.17533/udea.iatreia.v29n4a01Palabras clave:
cadeia avícola, Campylobacter spp., listeria monocytogenes , manipuladores de alimentos, Salmonella spp.Resumen
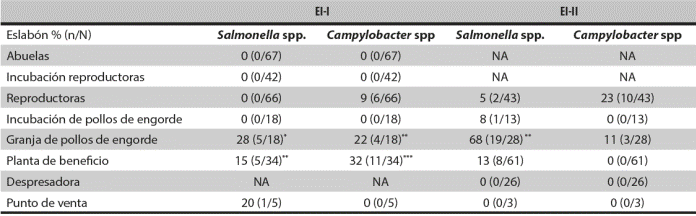
Salmonella spp., Campylobacter spp. y Listeria monocytogenes son patógenos zoonóticos causantes de enfermedades transmitidas por alimentos asociadas al consumo de productos de origen animal contaminados. En este estudio se determinaron la prevalencia y los factores de riesgo asociados a la presencia de estos microorganismos en todos los eslabones de producción de pollos de engorde en dos empresas integradoras avícolas colombianas (EI-I y EI-II). En la EI-I, se aislaron Campylobacter spp., y Salmonella spp., del 10 % y el 4,4 % de las muestras, y el serotipo predominante de esta última fue S. Heildelberg. Se encontró Salmonella spp., en 6 % de las muestras de manos y materia fecal de los trabajadores, y S. Saphra fue el serotipo más común.
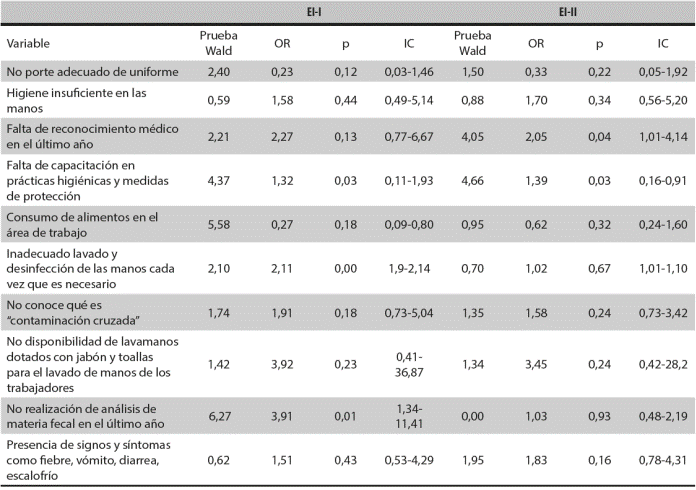
En la EI-II, la prevalencia de Campylobacter spp., y Salmonella spp., en muestras de animales fue del 7 % y el 17 %, respectivamente. No se detectó L. monocytogenes. Este trabajo estableció la prevalencia de los patógenos zoonóticos a lo largo de la cadena productiva, evidenció la presencia de trabajadores/manipuladores portadores de los patógenos y determinó, que “la falta de reconocimiento médico de los empleados en el último año” constituye un posible factor de riesgo para la portación de Salmonella spp.
Descargas
Citas
(1.) Grupo de vigilancia y control de factores de riesgo ambiental. Protocolo de vigilancia y control de enfermedades transmitidas por alimentos [Internet]. [consultado 2014 Sept 21]. Disponible en: http://www.minsalud.gov.co/comunicadosPrensa/Documents/ETA.pdf
(2.) Quinlan JJ. Foodborne illness incidence rates and food safety risks for populations of low socioeconomic status and minority race/ethnicity: a review of the literature. Int J Environ Res Public Health. 2013 Aug;10(8):3634-52. DOI 10.3390/ijerph10083634.
(3.) Mercado M, Avila J, Rey M, Montoya M, Gamboa A, Carrascal AK, et al. Brotes por Salmonella spp., Staphylococcus aureus y Listeria monocytogenes asociados al consumo de pollo. Biomédica. 2012 Jul-Sept;32(3):375-85. DOI 10.7705/biomedica.v32i3.697.
(4.) Zhao C, Ge B, De Villena J, Sudler R, Yeh E, Zhao S, et al. Prevalence of Campylobacter spp., Escherichia coli, and Salmonella serovars in retail chicken, turkey, pork, and beef from the Greater Washington, D.C., area. Appl Environ Microbiol. 2001 Dec;67(12):5431-6.
(5.) Sasaki Y, Haruna M, Murakami M, Hayashida M, Takahashi N, Urushiyama T, et al. Contamination of Poultry Products with Listeria monocytogenes at Poultry Processing Plants. J Vet Med Sci [Internet]. 2014 Jan [cited 2013 Jul 1]; 76(1):[129-32]. Available from: https://www.jstage.jst.go.jp/article/jvms/76/1/76_13-0267/_pdf
(6.) Scallan E, Hoekstra RM, Angulo FJ, Tauxe RV, Widdowson MA, Roy SL, et al. Foodborne illness acquired in the United States--major pathogens. Emerg Infect Dis. 2011 Jan;17(1):7-15. DOI 10.3201/eid1701.091101p1.
(7.) Grupo Enfermedades Transmisibles Equipo ETA. Protocolo de vigilancia en Salud Pública: Enfermedades Transmitidas por Alimentos (ETA) 2014 [Internet]. [consultado 2014 Sept 21]. Disponible en: http://www.ins.gov.co/lineas-de-accion/Subdireccion-Vigilancia/sivigila/Protocolos%20SIVIGILA/PRO%20Enfermedades%20Trans.%20por%20alimentos.pdf
(8.) Donado-Godoy P, Clavijo V, León M, Arevalo A, Castellanos R, Bernal J, et al. Counts, serovars, and antimicrobial resistance phenotypes of Salmonella on raw chicken meat at retail in Colombia. J Food Prot. 2014 Feb;77(2):227-35. DOI 10.4315/0362-028X.JFP-13-276.
(9.) Donado-Godoy P, Gardner I, Byrne BA, Leon M, Perez-Gutierrez E, Ovalle MV, et al. Prevalence, risk factors, and antimicrobial resistance profiles of Salmonella from commercial broiler farms in two important poultry-producing regions of Colombia. J Food Prot. 2012 May;75(5):874-83. DOI 10.4315/0362-028X.JFP-11-458.
(10.) Organización Mundial de Sanidad Animal. Pulorosis y tifosis aviar. En: Manual de la OIE sobre animales terrestres [Internet]. Paris: OIE; 2004. p. 937-8. [consultado 2015 Nov 17]. Disponible en: http://web.oie.int/esp/normes/mmanual/pdf_es/2.7.05_Pulorosis_y_tifosis_aviar.pdf
(11.) Callejo R, Prieto M, Martínez C, Aguerre L, Rocca F, Martínez G. Manual de procedimientos: Aislamiento, identificación y caracterización de Listeria monocytogenes 2008 [Internet]. [consultado 2013 Jul 1]. Disponible en: http://bvs.panalimentos.org/local/File/Manual_Listeria_monocytogenes_2008.pdf
(12.) United States Department of Agriculture. Isolation and Identification of Salmonella from Meat, Poultry, Pasteurized Egg, and Catfish Products and Carcass and Environmental Sponges [Internet]. [cited 2013 Jul 1]. Available from: http://www.fsis.usda.gov/wps/wcm/connect/700c05fe-06a2-492a-a6e1-3357f7701f52/MLG-4.pdf?MOD=AJPERES
(13.) Caffer MI, Terragno R. Manual de procedimientos para la caracterización de Salmonella [Internet]. [consultado 2013 Jul 1]. Disponible en: http://www.cdc.gov/ncidod/dbmd/gss/publications/documents/Argentina-LevelI/Manual_procedimientos_Salmonella.pdf
(14.) Grimont PA, Weill FX; WHO Collaborating Centre for Reference and Research on Salmonella. Antigenic formulae of the Salmonella serovars 2007. 9ª ed. [Internet]. [consultado 2013 Jul 1]. Disponible en: https://www.pasteur.fr/ip/portal/action/WebdriveActionEvent/oid/01s-000036-089
(15.) Muñoz ÁB, Chavez JA, Rodríguez EC, Realpe ME. Listeria monocytogenes en manipuladores de alimentos: un nuevo enfoque para tener en cuenta en los peligros de la industria alimentaria. Biomédica [Internet]. 2013 [consultado 2013 Jul 1]; 33:[283-91]. Disponible en: http://www.scielo.org.co/pdf/bio/v33n2/v33n2a14.pdfç
(16.) European Food Safety Authority. Scientific Opinion on a review on the European Union Summary Reports on trends and sources zoonoses, zoonotic agents and food-borne outbreaks in 2009 and 2010–specifically for the data on Salmonella, Campylobacter, verotoxigenic Escherichia coli, Listeria monocytogenes and foodborne outbreaks. EFSA Journal [Internet]. 2012 [cited 2013 Jul 1];10(6):[2726]. Available from: http://www.efsa.europa.eu/en/efsajournal/doc/2726.pdf
(17.) González LJ, Martínez FN, Rossi L, Tornese M, Troncoso A. Enfermedades transmitidas por los alimentos: Análisis del riesgo microbiológico. Rev Chil Infectol. 2010 Dic;27(6):513-24. DOI 10.4067/S0716-10182010000700004.
(18.) Pires SM, Vieira AR, Perez E, Wong DLF, Hald T. Attributing human foodborne illness to food sources and water in Latin America and the Caribbean using data from outbreak investigations. Int J Food Microbiol. 2012 Jan;152(3):129-38. DOI 10.1016/j.ijfoodmicro.2011.04.018.
(19.) Federación Nacional de Avicultores de Colombia [Internet]. Bogotá: FEVAVI; 2015 [consultado 2015 Jul 1]. Consumo Per Cápita. Disponible en: http://www.fenavi.org/index.php?option=com_content&view=article&id=2160&Itemid=556
(20.) Semana Sostenible [Internet]. Bogotá: Revista Semana; 2014 [consultado 2015 Jul 1]. CONtexto Ganadero. Carne de res, cerdo o pollo, ¿qué prefieren los colombianos? Disponible en: http://sostenibilidad.semana.com/consumo-responsable/articulo/carneres-cerdo-pollo-que-prefieren-colombianos/30562
(21.) Mohle-Boetani JC, Reporter R, Werner SB, Abbott S, Farrar J, Waterman SH, et al. An outbreak of Salmonella serogroup Saphra due to cantaloupes from Mexico. J Infect Dis. 1999 Oct;180(4):1361-4.
(22.) St Amand JA, Otto SJ, Cassis R, Annett Christianson CB. Antimicrobial resistance of Salmonella enterica serovar Heidelberg isolated from poultry in Alberta. Avian Pathol. 2013 Aug;42(4):379-86.
(23.) Donado-Godoy P, Castellanos R, León M, Arevalo A, Clavijo V, Bernal J, et al. The Establishment of the Colombian Integrated Program for Antimicrobial Resistance Surveillance (COIPARS): A Pilot Project on Poultry Farms, Slaughterhouses and Retail Market. Zoonoses Public Health. 2015 Apr;62 Suppl 1:58-69. DOI 10.1111/zph.12192.
(24.) Llarena AK, Huneau A, Hakkinen M, Hänninen ML. Predominant Campylobacter jejuni sequence types persist in Finnish chicken production. PLoS One. 2015 Feb;10(2):e0116585. DOI 10.1371/journal.pone.0116585.
(25.) Fajó-Pascual M, Godoy P, Ferrero-Cáncer M, Wymore K. Case-control study of risk factors for sporadic Campylobacter infections in northeastern Spain. Eur J Public Health. 2010 Aug;20(4):443-8. DOI 10.1093/eurpub/ckp206.
(26.) Mojica Pimiento A, Paredes Vega J. Centro Regional de estudios Económicos Bucaramanga. Características del sector avícola Colombiano y su reciente evolución en el Departamento de Santander [Internet]. [consultado 2015 Feb 27]. Disponible en: http://www.banrep.gov.co/sites/default/files/publicaciones/archivos/2005_agosto.pdf
(27.) Macari M, Mendes AA, Machado Menten JF, Nääs IA, editores. Boas Práticas de Produção. En: Produção de frangos de corte. 2a ed. São Paulo: FACTA; 2014. p. 440-63.
(28.) Green LR, Selman CA, Radke V, Ripley D, Mack JC, Reimann DW, et al. Food worker hand washing practices: an observation study. J Food Prot. 2006 Oct;69(10):2417-23.
Publicado
Cómo citar
Número
Sección
Licencia
Derechos de autor 2016 Iatreia

Esta obra está bajo una licencia internacional Creative Commons Atribución-CompartirIgual 4.0.
Los artículos publicados en la revista están disponibles para ser utilizados bajo la licencia Creative Commons, específicamente son de Reconocimiento-NoComercial-CompartirIgual 4.0 Internacional.
Los trabajos enviados deben ser inéditos y suministrados exclusivamente a la Revista; se exige al autor que envía sus contribuciones presentar los formatos: presentación de artículo y responsabilidad de autoría completamente diligenciados.