Prevalencia de anticuerpos contra Trypanosoma cruzi en mujeres embarazadas de zonas endémicas del departamento de Boyacá, Colombia
DOI:
https://doi.org/10.17533/udea.iatreia.v30n4a01Palabras clave:
Colombia, Enfermedad de Chagas, mujeres embarazadas, prevalenciaResumen
Objetivo: determinar la prevalencia de anticuerpos contra Trypanosoma cruzi en mujeres embarazadas de zonas endémicas del departamento de Boyacá en 2012 y 2013.
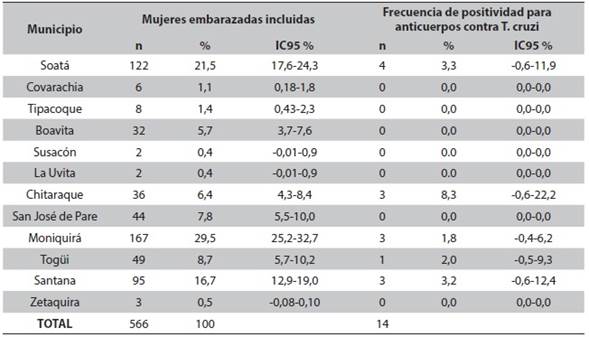
Materiales y métodos: estudio de corte transversal en 566 mujeres embarazadas procedentes de municipios de zona endémica para Chagas en este departamento. Las muestras se analizaron mediante las pruebas serológicas ELISA IgG para Chagas, Inmunofluorescencia indirecta y hemaglutinación indirecta. Se consideraron como confirmados los casos con resultados positivos en dos pruebas.
Resultados: la prevalencia global de anticuerpos contra Trypanosoma cruzi fue del 2,5 % (14/566). Los municipios con mayor prevalencia fueron Chitaraque (8,3 %) y Soatá (3,3 %). El promedio de edad de las mujeres positivas fue 32,6 años y el período gestacional, de 18,1 semanas. Se encontró asociación estadísticamente significativa entre la edad y la presencia de anticuerpos contra Trypanosoma cruzi.
Conclusión: la prevalencia de anticuerpos contra T. cruzi en mujeres embarazadas muestra la importancia del programa de vigilancia de Chagas gestacional, como una forma de controlar la enfermedad congénita.
Descargas
Citas
(1.) Parker ER, Sethi A. Chagas disease: coming to a place near you. Dermatol Clin. 2011 Jan;29(1):53-62. DOI 10.1016/j.det.2010.08.011.
(2.) Piat G, Almirón JF, Romano JR, Romano MF. Chagas congénito revisión de una enfermedad curable y subestimada. Rev Posgrado VIa Cátedra Med. 2009;(193):16-21.
(3.) Pérez-López FR, Chedraui P. Chagas disease in pregnancy: a non-endemic problem in a globalized world. Arch Gynecol Obstet. 2010 Dec;282(6):595-9. DOI 10.1007/s00404-010-1553-7.
(4.) Coura JR, Dias JC. Epidemiology, control and surveillance of Chagas disease: 100 years after its discovery. Mem Inst Oswaldo Cruz. 2009 Jul;104 Suppl 1:31-40.
(5.) Coura JR. Chagas disease: control, elimination and eradication. Is it possible? Mem Inst Oswaldo Cruz. 2013 Dec;108(8):962-7. DOI 10.1590/0074-0276130565.
(6.) Dias JC, Silveira AC, Schofield CJ. The impact of Chagas disease control in Latin America: a review. Mem Inst Oswaldo Cruz. 2002 Jul;97(5):603-12.
(7.) Organización Panamericana de la Salud. Estimación cuantitativa de la enfermedad de Chagas en las Américas [Internet]. Washington: OPS; 2006 [consultado 2014 May 23]. Disponible en: http://docplayer.es/12058322-Estimacion-cuantitativa-de-la-enfermedad-de-chagas-en-las-americas.html
(8.) Puerta CJ, Pavia PX, Montilla M, Flórez C, Herrera G, Ospina JM, et al. Reporte del primer caso de enfermedad de Chagas transplacentaria analizado por AP-PCR en Moniquirá, Boyacá. Biomédica. 2009;29(4):513-22. DOI 10.7705/biomedica.v29i4.125.
(9.) Cucunubá ZM, Valencia-Hernández CA, Puerta CJ, Sosa-Estani S, Torrico F, Cortés JA, et al. Primer consenso colombiano sobre Chagas congénito y orientación clínica a mujeres en edad fértil con diagnóstico de Chagas. Infectio. 2014 Abr-Jun;18(2):50-65. DOI 10.1016/j.infect.2013.12.001.
(10.) Instituto Nacional de Salud. Informe final del evento enfermedad de Chagas, Colombia 2014 [Internet]. Medellín: INS; 2014 [consultado 2015 Dic 10]. Disponible en: http://www.ins.gov.co/lineas-de-accion/Subdireccion-Vigilancia/Informe%20de%20Evento%20Epidemiolgico/Chagas%202014.pdf
(11.) Instituto Nacional de Salud. Informe final del evento enfermedad de Chagas, Colombia 2015 [Internet]. Medellín: INS; 2015 [consultado 2015 Dic 10]. Disponible en: http://www.ins.gov.co/lineas-de-accion/Subdireccion-Vigilancia/Informe%20de%20Evento%20Epidemiolgico/Chagas%202015.pdf
(12.) Instituto Nacional de Salud. Guía para la vigilancia por laboratorio de enfermedad de Chagas [Internet]. Medellín: INS; 2014 [consultado 2015 Dic 11]. Disponible en: http://www.ins.gov.co/tramites-y-servicios/examenes-de-interés-en-salud-publica/Parasitologa/GUIA%20VIGILANCIA%20POR%20LAB%20PARA%20CHAGAS.pdf
(13.) Campos-Valdez G, Canseco-Ávila LM, González-Noriega F, Alfaro-Zebadua O, Nava-Medecigo IY, Jiménez-Cardoso E. Transmisión materno-fetal de Trypanosoma cruzi, un problema de salud poco estudiado en México: caso Chiapas. Salud Publica Mex. 2016 May-Jun;58(3):378-84. DOI 10.21149/spm.v58i3.7898.
(14.) Lucero RH, Brusés BL, Merino DE, Fernández GJ, Crenna EC, Alonso JM. Enfermedad de Chagas congénito en Hospitales de la ciudad de Corrientes-Argentina. Enf Emerg. 2007 Jul-Sep;9(3):121-4.
(15.) Otero S, Sulleiro E, Molina I, Espiau M, Suy A, Martín-Nalda A, et al. Congenital transmission of Trypanosoma cruzi in non-endemic areas: evaluation of a screening program in a tertiary care hospital in Barcelona, Spain. Am J Trop Med Hyg. 2012 Nov;87(5):832-6. DOI 10.4269/ajtmh.2012.12-0152.
(16.) Cucunubá ZM, Flórez AC, Cárdenas A, Pavía P, Montilla M, Aldana R, et al. Prevalence and risk factors for Chagas disease in pregnant women in Casanare, Colombia. Am J Trop Med Hyg. 2012 Nov;87(5):837-42. DOI 10.4269/ajtmh.2012.12-0086.
(17.) Manrique-Abril F, Ospina JM, Herrera G, Florez AC, Pavia PX, Montilla M, et al. Diagnóstico de enfermedad de Chagas en mujeres embarazadas y recién nacidos de Moniquirá y Miraflores, Boyacá, Colombia. Infectio. 2013 Ene-Mar;17(1):28-34. DOI 10.1016/S0123-9392(13)70045-6.
(18.) Salas Clavijo NA, Postigo JR, Schneider D, Santalla JA, Brutus L, Chippaux JP. Prevalence of Chagas disease in pregnant women and incidence of congenital transmission in Santa Cruz de la Sierra, Bolivia. Acta Trop. 2012 Oct;124(1):87-91. DOI 10.1016/j.actatropica.2012.06.012.
(19.) Ortiz S, Zulantay I, Solari A, Bisio M, Schijman A, Carlier Y, et al. Presence of Trypanosoma cruzi in pregnant women and typing of lineages in congenital cases. Acta Trop. 2012 Dec;124(3):243-6. DOI 10.1016/j.actatropica.2012.08.001.
(20.) Mendoza Ticona CA, Córdova Benzaquen E, Ancca Juárez J, Saldaña Díaz J, Torres Choque A, Velásquez Talavera R, et al. Prevalencia de la enfermedad de Chagas en puérperas y transmisión congénita en una zona endémica del Perú. Rev Panam Salud Publica. 2005;1(3):147-53.
(21.) Muñoz-Vilches MJ, Salas J, Cabezas T, Metz D, Vázquez J, Soriano MJ. [Chagas screening in pregnant Latin-American women. Experience in Poniente Almeriense (Almeria, Spain)]. Enferm Infecc Microbiol Clin. 2012 Aug;30(7):380-2. DOI 10.1016/j.eimc.2011.11.012.
(22.) Monroy ÁL, Pedraza AM, Prada CF. Prevalencia de anticuerpos anti-Trypanosoma cruzi en mujeres en edad fértil en Socotá, Boyacá, 2014. Biomédica. 2016; 36 supl 1: 90-6. DOI 10.7705/biomedica.v36i3.2923.
(23.) Bern C, Verastegui M, Gilman RH, Lafuente C, Galdos-Cardenas G, Calderon M, et al. Congenital Trypanosoma cruzi transmission in Santa Cruz, Bolivia. Clin Infect Dis. 2009 Dec;49(11):1667-74. DOI 10.1086/648070.
(24.) Torrico F, Alonso-Vega C, Suarez E, Rodriguez P, Torrico MC, Dramaix M, et al. Maternal Trypanosoma cruzi infection, pregnancy outcome, morbidity, and mortality of congenitally infected and non-infected newborns in Bolivia. Am J Trop Med Hyg. 2004 Feb;70(2):201-9.
Publicado
Cómo citar
Número
Sección
Licencia
Derechos de autor 2017 Iatreia

Esta obra está bajo una licencia internacional Creative Commons Atribución-CompartirIgual 4.0.
Los artículos publicados en la revista están disponibles para ser utilizados bajo la licencia Creative Commons, específicamente son de Reconocimiento-NoComercial-CompartirIgual 4.0 Internacional.
Los trabajos enviados deben ser inéditos y suministrados exclusivamente a la Revista; se exige al autor que envía sus contribuciones presentar los formatos: presentación de artículo y responsabilidad de autoría completamente diligenciados.