Recuento de células CD34+ en sangre periférica como predictor de adecuada recolección de progenitores hematopoyéticos para trasplante autólogo
DOI:
https://doi.org/10.17533/udea.iatreia.v29n4a04Palabras clave:
Colombia , eliminación de componentes sanguíneos, factores de crecimiento de célula hematopoyética, linfoma, mieloma múltiple, trasplante de médula óseaResumen
Introducción: para llevar a cabo un trasplante autólogo se deben movilizar los progenitores hematopoyéticos a la sangre periférica y posteriormente recolectarlos por aféresis. El recuento de células CD34+ es una herramienta para determinar el mejor momento para la recolección.
Objetivo: evaluar la asociación entre el recuento de células CD34+ en sangre periférica y la recolección exitosa de progenitores hematopoyéticos.
Materiales y métodos: evaluación de una prueba predictiva para determinar la utilidad del recuento de células CD34+ en sangre periférica como predictor del éxito de la recolección de progenitores hematopoyéticos en pacientes a los que se les va a hacer un trasplante autólogo.
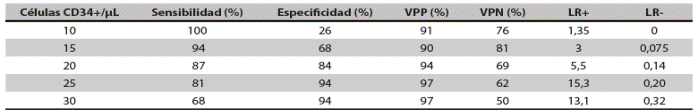
Resultados: se incluyó a 77 pacientes (mediana de edad: 49 años; rango: 5-66); el diagnóstico predominante fue linfoma (53,2 %). El porcentaje de pacientes con recolección exitosa de progenitores fue proporcional al número de células CD34+ en sangre periférica al finalizar la movilización. Proponemos que se deben tener más de 15 células CD34+/μL en sangre periférica para lograr una adecuada recolección de progenitores hematopoyéticos.
Conclusión: el recuento de células CD34+ en sangre periférica es una herramienta útil para predecir la recolección exitosa de progenitores hematopoyéticos.
Descargas
Citas
(1.) Demirer T, Bensinger WI, Buckner CD. Peripheral blood stem cell mobilization for high-dose chemotherapy. J Hematother. 1999 Apr;8(2):103-13.
(2.) Bensinger W, DiPersio JF, McCarty JM. Improving stem cell mobilization strategies: future directions. Bone Marrow Transplant. 2009 Feb;43(3):181-95. DOI 10.1038/bmt.2008.410.
(3.) Gertz MA. Current status of stem cell mobilization. Br J Haematol. 2010 Sep;150(6):647-62. DOI 10.1111/j.1365-2141.2010.08313.x.
(4.) Damon L, Damon LE, Gaensler K, Kaplan L, Martin T 3rd, Rubenstein J, et al. Impact of intensive PBSC mobilization therapy on outcomes following auto-SCT for non-Hodgkin’s lymphoma. Bone Marrow Transplant. 2008 Nov;42(10):649-57. DOI 10.1038/bmt.2008.236.
(5.) Mehta J, Oyama Y, Winter J, Williams S, Tallman M, Singhal S, et al. CD34(+) cell collection efficiency does not correlate with the pre-leukapheresis hematocrit. Bone Marrow Transplant. 2001 Sep;28(6):597-601. DOI 10.1038/sj.bmt.1703197.
(6.) Malik S, Bolwell B, Rybicki L, Copelan O, Duong H, Dean R, et al. Apheresis days required for harvesting CD34+ cells predicts hematopoietic recovery and survival following autologous transplantation. Bone Marrow Transplant. 2011 Dec;46(12):1519-25. DOI 10.1038/bmt.2010.336.
(7.) Camacho Villa AY, Reyes Maldonado E, Montiel Cervantes LA, Vela Ojeda J. CD133+CD34+ and CD133+CD38+ blood progenitor cells as predictors of platelet engraftment in patients undergoing autologous peripheral blood stem cell transplantation. Transfus Apher Sci. 2012 Jun;46(3):239-44. DOI 10.1016/j.transci.2012.02.002.
(8.) Rowley SD, Yu J, Gooley T, Heimfeld S, Holmberg L, Maloney D, et al. Trafficking of CD34+ cells into the peripheral circulation during collection of peripheral blood stem cells by apheresis. Bone Marrow Transplant. 2001 Oct;28(7):649-56.
(9.) Copelan EA. Hematopoietic stem-cell transplantation. N Engl J Med. 2006 Apr;354(17):1813-26.
(10.) Duong HK, Savani BN, Copelan E, Devine S, Costa LJ, Wingard JR, et al. Peripheral blood progenitor cell mobilization for autologous and allogeneic hematopoietic cell transplantation: guidelines from the American Society for Blood and Marrow Transplantation. Biol Blood Marrow Transplant. 2014 Sep;20(9):1262-73. DOI 10.1016/j.bbmt.2014.05.003.
(11.) Yu J, Leisenring W, Bensinger WI, Holmberg LA, Rowley SD. The predictive value of white cell or CD34+ cell count in the peripheral blood for timing apheresis and maximizing yield. Transfusion. 1999 May;39(5):442-50.
(12.) Schots R, Van Riet I, Damiaens S, Flament J, Lacor P, Staelens Y, et al. The absolute number of circulating CD34+ cells predicts the number of hematopoietic stem cells that can be collected by apheresis. Bone Marrow Transplant. 1996 Apr;17(4):509-15.
(13.) Gutensohn K, Magens MM, Kuehnl P, Zeller W. Increasing the economic efficacy of peripheral blood progenitor cell collections by monitoring peripheral blood CD34+concentrations. Transfusion. 2010 Mar;50(3):656-62. DOI 10.1111/j.1537-2995.2009.02466.x.
(14.) Pérez-Simón JA, Caballero MD, Corral M, Nieto MJ, Orfao A, Vazquez L, et al. Minimal number of circulating CD34+ cells to ensure successful leukapheresis and engraftment in autologous peripheral blood progenitor cell transplantation. Transfusion. 1998 Apr;38(4):385-91.
(15.) Remes K, Matinlauri I, Grenman S, Itälä M, Kauppila M, Pelliniemi TT, et al. Daily measurements of blood CD34+ cells after stem cell mobilization predict stem cell yield and posttransplant hematopoietic recovery. J Hematother. 1997 Feb;6(1):13-9.
(16.) Narayanasami U, Kanteti R, Morelli J, Klekar A, Al-Olama A, Keating C, et al. Randomized trial of filgrastim versus chemotherapy and filgrastim mobilization of hematopoietic progenitor cells for rescue in autologous transplantation. Blood. 2001 Oct;98(7):2059-64.
(17.) Körbling M, Freireich EJ. Twenty-five years of peripheral blood stem cell transplantation. Blood. 2011 Jun;117(24):6411-6. DOI 10.1182/blood-2010-12-322214.
(18.) Nese Ravazzani MC, Guillermo Espósito MC, Díaz Filgueira L, Isaurralde Delsart HR, Grinberg Weissman S, Perdomo Martínez AM, et al. Trasplante autólogo con progenitores hematopoyéticos (auto-tph). Evaluación de 1995 a 2001. Arch Med Interna (Montevideo). 2001 Dic;23(4):187-93.
Publicado
Cómo citar
Número
Sección
Licencia
Derechos de autor 2016 Iatreia

Esta obra está bajo una licencia internacional Creative Commons Atribución-CompartirIgual 4.0.
Los artículos publicados en la revista están disponibles para ser utilizados bajo la licencia Creative Commons, específicamente son de Reconocimiento-NoComercial-CompartirIgual 4.0 Internacional.
Los trabajos enviados deben ser inéditos y suministrados exclusivamente a la Revista; se exige al autor que envía sus contribuciones presentar los formatos: presentación de artículo y responsabilidad de autoría completamente diligenciados.