Técnica de plastinación de la Universidad de Antioquia: una adaptación del método estándar alemán
DOI:
https://doi.org/10.17533/udea.iatreia.v31n3a01Palabras clave:
conservación, docencia, laboratorio, modelos anatómicos, morfologíaResumen
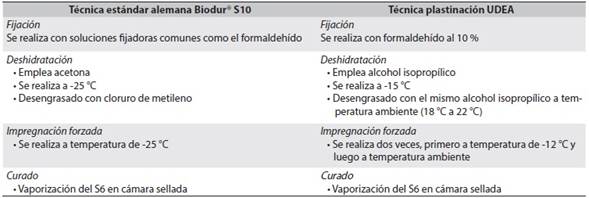
Introducción: la plastinación es una técnica de conservación de componentes anatómicos que consiste en reemplazar las moléculas de agua por un polímero. Esto se logra en cuatro etapas (fijación, deshidratación, impregnación forzada y curado). Con base en ello nuestro objetivo fue adaptar el método estándar alemán, a las condiciones propias del Laboratorio de Plastinación de la Facultad de Medicina de la Universidad de Antioquia (UDEA).
Materiales y métodos: se adaptó el método estándar alemán al reemplazar el agente deshidratante original, la acetona, por alcohol isopropílico. Fue necesario modificar la temperatura de la etapa de impregnación forzada en la técnica estándar alemana, realizada en su totalidad en frío. Esto hace que la técnica adaptada requiera realizar una segunda impregnación a temperatura ambiente.
Resultados: se han obtenido 343 piezas plastinadas, de estas, 150 mediante el protocolo de plastinación UDEA, con las características descritas en el método estándar alemán: secas, inodoras, de aspecto natural y duradero.
Discusión: aunque la técnica de plastinación de la UDEA aumenta el consumo de polímeros, es favorable en la relación costo/beneficio, pues disminuye los costos respecto a la aplicación de la técnica estándar alemana en nuestro medio. Emplear piezas plastinadas para la enseñanza tiene distintas ventajas. Permite reemplazar el uso de la conservación de piezas a base de formaldehído, evitando la exposición al mismo y sus efectos nocivos para la salud; por lo cual el uso de la misma ha ayudado a fortalecer diversos programas académicos en nuestra facultad.
Descargas
Citas
(1.) Beltrán Guerra JA. Historia de la preservación de cadáveres humanos. Morfolia. 2009;1(3):5-10.
(2.) Pashaei S. A brief review on the history, methods and applications of platination. Int J Morphol [Internet]. 2010; 28(4):1075-9. Available from: https://pdfs.semanticscholar.org/045e/65129819f365260a3bad87fd769326e8f716.pdf
(3.) von Hagens G. Heidelberg plastination folder: Collection of al technical leaflets for plastination. 2nd ed. Heidelberg: Biodur Products; 1986.
(4.) Bickley HC, von Hagens G, Townsend FM. An improved method for the preservation of teaching specimens. Arch Pathol Lab Med. 1981 Dec;105(12):674-6.
(5.) Latorre R, Vásquez JM, Gil F, Ramirez G, López-Albors O, Orenes M, et al. Teaching anatomy of the distal equine thoracic limb whit plastined slices. J Int Soc Plastination [Internet]. 2001;16:23-30. Available from: http://plastination.org/journal/archive/jp_vol.16/jp_vol.16_23-30.pdf
(6.) von Hagens G. Impregnation of soft biological specimens with thermosetting resins and elastomers. Anat Rec. 1979 Jun; 94(2):247-55. DOI 10.1002/ar.1091940206.
(7.) von Hagens G, Tiedemann K, Kriz W. The current potential of plastination. Anat Embryol (Berl). 1987;175(4):411-21.
(8.) Bickley HC, Conner RS, Walker AN, Jackson RL. Preservation of tissue by silicone rubber impregnation. J Int Soc Plastination 1987;1(1):30-9.
(9.) Sora MC, Cook P. Epoxy plastination of biological tissue: E12 technique. J Int Soc Plastination [Internet]. 2007;22:31-9. Available from: http://journal.plastination.org/archive/jp_vol.22/jp_vol.22_31-39.pdf
(10.) Sora MC. Epoxy plastination of biological tissue: E12 ultra-thin technique. J Int Soc Plastination [Internet]. 2007;22:40-5. Available from: https://www.yumpu.com/en/document/view/5151787/epoxy-plastination-of-biological-tissue-e12-ultra-thin-technique
(11.) Latorre R, Henry RW. Polyester plastination of biological tissue: P40 technique for body slices. J Int Soc Plastination. 2007; 22:69-77.
(12.) Henry RW, Latorre R. Polyester plastination of biological tissue: P40 technique for brain slices. J Int Soc Plastination [Internet]. 2007; 22:59-68. Available from: http://journal.plastination.org/archive/jp_vol.22/jp_vol.22_59-68.pdf
(13.) Weber WA, Weiglein A, Latorre R, Henry RW. Polyester plastination of biological tissue: P35 technique. J Int Soc Plastination. 2007;22:50-8.
(14.) Dejong K, Henry RW. Silicone plastination of biological tissue: Cold-temperature technique biodurtm s10/s15 technique and products. J Int Soc Plastination. 2007;22:2-14.
(15.) Raoof A, Henry RW, Reed RB. Silicone plastination of bilogical tissue: room-temperature technique dowtm/corcoran technique and products. J Int Soc Plastination [Internet]. 2007;22:21-5. Available from: http://journal.plastination.org/archive/jp_vol.22/jp_vol.22_21-25.pdf
(16.) Henry RW. Silicone plastination of biological tissue: Cold-temperature technique- North Carolina technique and products. J Int Soc Plastination. 2007;22:26-30.
(17.) Robert H, Larry J, Carol H. Specimen preparation for silicone plastination. J Int Soc Plastination [Internet]. 1997;12(1):13-7. Available from: http://plastination.org/journal/archive/jp_vol.12.1/jp_vol.12.1_13-17.pdf
(18.) Baker EW, Slott PA, Terracio L, Cunningham EP. An innovative method for teaching anatomy in the predoctoral dental curriculum. J Dent Educ. 2013 Nov;77(11):1498-507.
(19.) Pandit S, Kumar S, Mishra BK. Comparative study of anatomical specimens using plastination by araldite HY103, polypropylene resin, 6170H19 Orthocryl and silicone - A qualitative study. Med J Armed Forces India. 2015 Jul;71(3):246-53. DOI 10.1016/j.mjafi.2015.04.014.
(20.) Ottone NE, Cirigliano V, Bianchi HF, Medan CD, Algieri RD, Borges Brum G, et al. New contributions to the development of a plastination technique at room temperature with silicone. Anat Sci Int. 2015 Mar;90(2):126-35. DOI 10.1007/s12565-014-0258-6.
(21.) Miranda F. La plastinación como método de conservación de tejidos biológicos para docencia e investigación en la anatomía humana. Rev Peru Med Exp Salud Publica [Internet]. 2015;32(4):817-24. Disponible en: http://www.scielo.org.pe/pdf/rins/v32n4/a30v32n4.pdf
(22.) Arredondo J, López-Albors O, Recillas S, Victoria M, Castelán O, González-Ronquillo M, et al. Modelo virtual tridimensional de la articulación cubital del perro a partir de cortes plastinados ultradelgados. Int J Morphol [Internet]. 2016;34 (4):1253-8. Disponible en: http://www.scielo.cl/pdf/ijmorphol/v34n4/art13.pdf
(23.) McRae KE, Davies GA, Easteal RA, Smith GN. Creation of plastinated placentas as a novel teaching resource for medical education in obstetrics and gynaecology. Placenta. 2015 Jul; 36(9):1045-51. DOI 10.1016/j.placenta.2015.06.018.
(24.) Zheng TZ, You X, Cai L, Liu J. The history of plastination in china. J Int Soc Plastination [Internet]. 2000;15(1):25-9. Disponible en: http://journal.plastination.org/archive/jp_vol.15/jp_vol.15_25-29.pdf
(25.) Jiménez Mejia R, Isaza Castro O. Plastinación, una técnica moderna al servicio de la anatomía. Iatreia [Internet]. 2005;18(1):99-106. Disponible en: https://aprendeenlinea.udea.edu.co/revistas/index.php/iatreia/article/view/4134/3797
(26.) Colombia. Congreso de Colombia. Ley 919 de 2004 por medio de la cual se prohíbe la comercialización de componentes anatómicos humanos para trasplante y se tipifica como delito su tráfico. Diario Oficial, 45771 (Dic. 23 2004).
(27.) Colombia. Ministro de la Protección Social. Decreto 2493 de 2004 por el cual se reglamentan parcialmente las Leyes 9ª de 1979 y 73 de 1988, en relación con los componentes anatómicos. Diario Oficial, 45631 (Ago. 05 2004).
(28.) Colombia. Ministerio de la Protección Social. Resolución 002640 de 2005 por medio de la cual se reglamentan los artículos 3º, 4º, 6º parágrafo 2º, 7º numeral 10, 25 y 46 del Decreto 2493 de 2004 y se dictan otras disposiciones. Diario Oficial, 46007 (Ago. 21 2005).
(29.) Colombia. Ministerio de Protección Social. Resolución 0042 de 2008, por la cual se modifica el artículo 20 de la Resolución 2640 de 2005. Diario Oficial, 46894 (Feb. 06 2008).
(30.) Pabst R. Exposure to formaldehyde in anatomy: an occupational health hazard? Anat Rec. 1987 Oct;219(2):109-12.
(31.) Viegas S, Ladeira C, Nunes C, Malta-Vacas J, Gomes M, Brito M, et al. Genotoxic effects in occupational exposure to formaldehyde: A study in anatomy and pathology laboratories and formaldehyde-resins production. J Occup Med Toxicol. 2010 Aug;5(1):25. DOI 10.1186/1745-6673-5-25.
(32.) Alcaldía de Medellín [Internet]. Alcaldía: Medellín; 2017 [consultado 2017 agosto 1]. Disponible en: https://www.medellin.gov.co/irj/portal/medellin?navigationtarget=navurl://6488ef50a6787e1fdbc4e42e62a46a67
(33.) Hopwood D. Fixatives and fixation: a review. Histochem J. 1969 May;1(4):323-60.
(34.) Brenner E. Human body preservation - old and new techniques. J Anat. 2014 Mar;224(3):316-44. DOI 10.1111/joa.12160.
(35.) Colombia. Consejo Nacional de Estupefacientes. Resolución 0001 de 2015, por la cual se unifica y actualiza la normatividad sobre el control de sustancia y productos químicos. Bogotá: Consejo Nacional de Estupefacientes; 08 enero de 2015.
(36.) Brown MA, Reed RB, Henry RW. Effects of dehydration mediums and temperature on total dehydration time and tissue shrinkage. J Int Soc Plastination [Internet]. 2002;17:28-33. Available from: http://www.plastination.org/journal/archive/jp_vol.17/jp_vol.17_28-33.pdf
(37.) Chang R. Fuerzas intermoleculares y líquidos y sólidos. En: Química. 10a ed. México D.F: Mc Graw Hill; 2010. p. 460-511.
(38.) Ruthig VA, Labrash S, Lozanoff S, Ward MA. Macroscopic demonstration of the male urogenital system with evidence of a direct inguinal hernia utilizing room temperature plastination. Anatomy. 2016 Dec;10(3):211-20. DOI 10.2399/ana.16.036.
(39.) Riederer BM. Plastination and its importance in teaching anatomy. Critical points for long-term preservation of human tissue. J Anat. 2014 Mar;224(3):309-15. DOI 10.1111/joa.12056.
(40.) Ottone NE, Cirigliano V, Lewicki M, Bianchi HF, Aja-Guardiola S, Algieri RB, et al. Plastination Technique in Laboratory Rats: an Alternative Resource for Teaching, Surgical Training and Research Development. Int J Morphol. 2014;32(4):1430-5. Available from: http://www.scielo.cl/pdf/ijmorphol/v32n4/art48.pdf
(41.) Aronson JK. Formaldehyde. In: Lisa Tickner. Meyler’s side effects of drugs. 6th ed. Amsterdam: Elsevier; 2016. p. 437-43.
Publicado
Cómo citar
Número
Sección
Licencia
Derechos de autor 2018 Iatreia

Esta obra está bajo una licencia internacional Creative Commons Atribución-CompartirIgual 4.0.
Los artículos publicados en la revista están disponibles para ser utilizados bajo la licencia Creative Commons, específicamente son de Reconocimiento-NoComercial-CompartirIgual 4.0 Internacional.
Los trabajos enviados deben ser inéditos y suministrados exclusivamente a la Revista; se exige al autor que envía sus contribuciones presentar los formatos: presentación de artículo y responsabilidad de autoría completamente diligenciados.